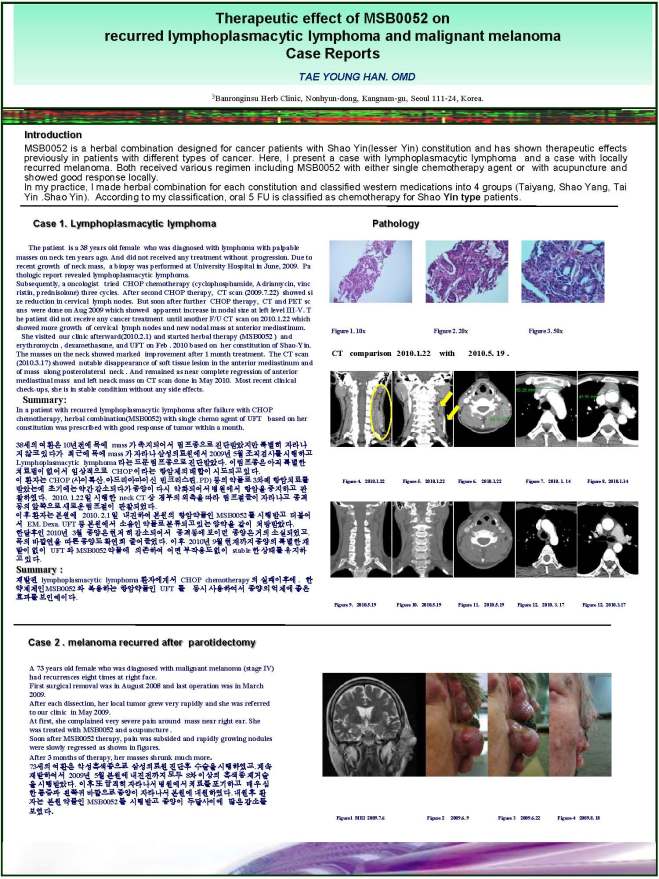
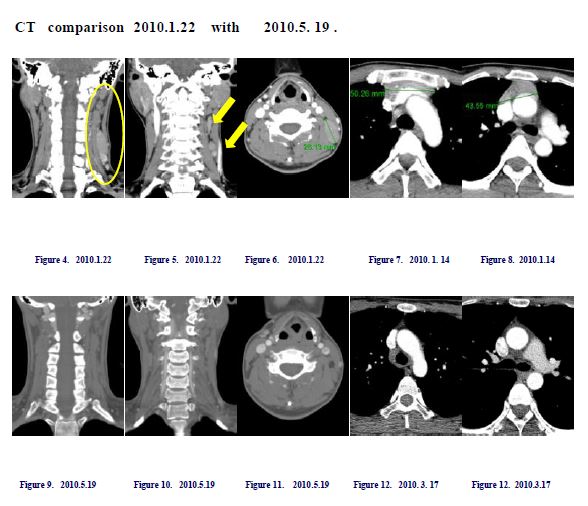
본인이 사상의학적으로 주장하는 항암제는 체질에 따라서 사용해야 하고 체질이 안 맞을 때는 오히려 항암제가 암을 더 빨리 퍼뜨릴 수 있다는 주장에 대해서, 최신 미국에서 연구된 택솔이 유방암 환자의 폐전이를 악화시킬 수 있고 촉발할 수 있다는 주장을 연구한 기사를 소개해 본다. 나중에 이 논문을 자세히 보고 실어보려고 하는데 독자들은 유방암 14강의 환자가 소음인 체질로 택솔을 매주 1회 12 차를 사용하고 나서 폐전이 뼈전이가 된 경우를 보았을 것이다. 이 부분을 같이 연결시켜서 생각해 보면 알 수 있으리라 본다.
http://health.chosun.com/news/dailynews_view.jsp?mn_idx=197500
널리 사용되는 항암화학제 약물이 실제로 암 세포가 퍼지게 할 수 있는 것으로 나타났다.
8일 오하이오주립대학 연구팀이 미국립과학원보’에 발표한 새로운 연구결과에 의하면 항암화학제의 부작용들로 인해 유방암이 퍼질 수 있는 것으로 나타났다.
최근 들어 항암제의 효능의 진보로 인해 유방암 생존율은 최근 몇 년 내 계속 향상되고 있다. 하지만 이전 연구들에 의하면 유방암 치료에 사용되는 항암화학제가 전이 위험을 높이는 것으로 나타난 바 있다.
실제로 올 초 발표된 한 연구에 의하면 유방암에서의 항암화학요법이 유방암을 앓는 쥐와 소규모의 유방암 환자에서 세포 수준에서 변화를 유발할 수 있는 것으로 나타난 바 있다.
이번 연구결과 파클리탁셀(paclitaxel)이라는 유방암, 폐암, 난소암 등 각종 암 치료에 널리 사용되는 항암화학제가 유방암 세포들이 폐로 퍼지게 하는 것으로 나타났다.
실제로 파클리탁셀이 스트레스에 의해 활성화되는 전사인자인 Atf3이라는 유전자 과발현을 유발할 수 있어 이로 인해 폐 내 암 세포 친화 환경을 만들어 유방암이 전이되게 하는 것으로 나타났다.
연구팀은 “파클리탁셀이 유방암 치료에 도움이 될 수 있을 뿐 아니라 암이 퍼지게도 할 수 있다”라고 강조했다.
- * Copyright ⓒ 메디컬투데이 All Rights Reserved.
- * 본 기사의 내용은 헬스조선의 편집방향과 일치하지 않을 수도 있습니다.
오하이오 주립대 원문.
https://news.osu.edu/news/2017/08/07/chemo-paradox/
화학 요법이 암이 유방에서 폐로 퍼지는 것을 도와준다.
마우스 연구는 파클리탁셀의 역설적인 전립선 암 효과를 설명하는 데 도움이 됩니다.
작성자 : Misti Crane
2017 년 8 월 7 일 발행 ( 구글번역인용)
오하이오 주 콜럼버스 – 유방암을 억제하는 똑같은 치료법이 또하나의 어두운 면을 가지고 있다. 즉 이는 유방암을 치료함과 동시에 폐에 암전이의 확산을 도와주는 연료 역할을 한다.
오하이오 주립 대학 (Ohio State University)의 연구자들은 전이성 암으로 이어지는 사건의 계단식을 연구하여 항암약물이 유방 조직에서 암과 싸우는 성질을 보존하면서 언젠가 약품의 단점을 억제할 수 있는 가능성을 열어 준 단서를 발견했습니다.
유방암의 표준 화학요법 약물인 파클리탁셀은 유방암 세포가 원발종양에서 벗어나서 다른 곳으로 전이 될 수 있는 다양한 분자 수준의 변화를 일으킨다. 연구자들은 유방암의 마우스 모델에서택솔이 암세포들이 폐로 쉽게 퍼질 수 있도록 하는 이 질병의 확산을 촉진하는 우호적인 환경을 만드는 것을 발견했다.
미국 국립 과학 아카데미 (National Academy of Sciences) 지에 발표된 이번 연구는 마우스 모델의 결과가 유방암 전이와 관련이 있음을 암시하는 유방암 여성의 데이터 분석을 같이 포함시켰다.
 |
| Tsonwin Hai |
” 화학 요법이 역설적으로 암 진행을 촉진시킬 수 있다는 것은 , 암 연구에서의 새로운 비존이 나타나고 있다. 그러나 이 충격적인 화학약물의 악 영향에 대한 분자 수준의 이해는 명확하지 않다 “고 연구의 수석 저자이자 생물 화학 및 약리학 교수 인 Tsonwin Hai는 말했다 .
이연구에서 언급된 종양과 폐의 변화의 요점은 바로 스트레스에 의해 스위치가 켜지는 Atf3라는 유전자에 달려 있다. 인간 데이터에서 연구자들은 화학 요법을 받은 환자들이 화학요법을 받지 않은 환자들 보다 Atf3 유전자 발현이 높다는 것을 발견했다.
“이 유전자는 즉시 두 가지 역할을 하는 것처럼 보인다 : 본질적으로 ‘씨앗'(암세포)을 분배하고 ‘토양'(폐의 암이 퍼지는 환경)을 비옥하게 하는 데 도움이 된다.
첫째, 화학 요법은 암세포가 원발 종양에서 빠져나와서 혈류로 타고 다른 장기로 이동하게 하는 분자들이 원발성 종양에서 탈출 할 수 있는 분자 문 (molecular doors)의 수를 늘리기 위한 신호를 보내는 것으로 나타났다.
“나는 이것이 암 세포가 새는 혈관 때문에 혈류에 들어가는 수동적 과정보다는 암 세포가 혈액으로 빠져 나오도록 촉구하는 능동적인 생물학적 변화라고 생각한다”고 Hai 교수는 말했다. 오하이오 주립 대학 종합 암 센터
“이 발견은 알버트 아인슈타인 의과 대학에서 진행되어 Scienc Translational Medicine 에 발표된 유사한 결과를 보여주는 이미징 기술을 사용하여 생쥐의 종양을 관찰 한 또다른 연구에 의해 이 이론이 뒷받침 되었다고 본다” 라고 연구자인 하이는 말했습니다.
둘째, 오하이오주의 연구자들은 암세포가 빠져나가는 것을 돕는 것 이상으로 파클리탁셀이 폐암의 조직 환경을 비옥한 토양이 되게 하여 암세포 들이 잘 순환할 수 있도록 하는 일련의 사건을 일으킨다는 것을 발견했다.
하이는 “파크리탁셀이라는 항암제가 암세포가 폐에 들어가서 쉽게 뿌리밖고 자랄수 있는 신호를 보냄으로써, 면역학적으로 암세포에 훨씬 관대한 환경을 폐에 만들어 준다. “라고 말했다.
화학 요법이 때때로 전이성 암의 위험을 증가시키는지에 대한 분자 수준의 이해는 초기 단계에 있다고 하이는 말했다.
그녀는 연구의 마우스 모델에서 암 세포가 매우 공격적이며 ,파크리탁셀이 암 진행의 초기 단계에서 암 세포의 도피를 강화하는지 여부를 테스트는 매우 흥미롭고 중요하다라고 말했다.
Hai는 암의 확산에 대한 mouse model 의 결과를 가지고 인간의 암치료에 대해 추론하기 위해서는 에 훨씬 더 많은 연구가 필요하다고 경고했다.
“이 시점에서 우리의 연구와 화학 요법에 대한 최근에 연구된 문헌에서 알 수 있듯이 – 우리는 화학 요법이 암 치료에 도움이 되는 동시에 암의 확산 가능성을 증가시킬 수 있다는 관점에 대해 신중하게 우리의 마음을 열어 두는 것이 현명하다.” 라고 그녀가 말했다.
이 분야의 다른 연구와 차별화된 연구는 스트레스 유전자 Atf3의 동정입니다. 그들은 파클리탁셀이 스트레스의 원인으로 – 적어도 부분적으로 Atf3 유전자를 스위치를 켜서 암의 확산을 촉진하는 것을 보여주었습니다.
” 화학요법과 함께 스트레스 유전자 Atf3의 효과를 약화시키는 방법을 같이 시행하므로써 이 문제를 풀 가능성이 있다”고 Hai 씨는 말했다.
그리고 연구자 하이(Hai)는 앞으로 이분야를 연구의 촛점으로 삼고 연구하게 될것이라고 말했다.
미 국방부는이 연구를 지원했습니다.
이 연구에 참여한 다른 오하이오 주 연구원은 장이석 (Yi Seok Chang), 스와티 (Swati Jalgaonkar), 저스틴 미들턴 (Justin Middleton)들입니다.
How a chemo drug can help cancer spread from the breast to the lungs
Mouse study helps explain the paradoxical pro-cancer effects of paclitaxel
By: Misti Crane
Published on August 07, 2017
COLUMBUS, Ohio –The very same treatment that thwarts breast cancer has a dark side – it can fuel the spread of the disease to the lungs.
Researchers at The Ohio State University studied the cascade of events that lead to metastatic cancer and found clues to why it happens, opening up the possibility of one day interfering with the medication’s downsides while preserving its cancer-fighting properties in breast tissue.
The front-line chemotherapy drug paclitaxel sets off a variety of molecular-level changes that allow breast cancer cells to escape from the tumor. At the same time, it creates an environment in the lung that is more hospitable to the cancer cells, facilitating the spread of the disease, the researchers found in a mouse model of breast cancer.
The study, which appears in the journal Proceedings of the National Academy of Sciences, includes an analysis of data from women with breast cancer that suggest the findings from mouse models could be relevant to breast cancer metastasis in humans.
 |
| Tsonwin Hai |
“That chemotherapy can paradoxically promote cancer progression is an emerging revelation in cancer research. However, a molecular-level understanding of this devastating effect is not clear,” said Tsonwin Hai, the study’s senior author and a professor of biological chemistry and pharmacology.
The changes in both the tumor and the lung documented in the study depend on a gene called Atf3, which is turned on by stress. In human data, the researchers found higher Atf3 gene expressionin patients who had chemotherapy than those who did not.
“This gene seems to do two things at once: essentially help distribute the ‘seeds’ (cancer cells) and fertilize the ‘soil’ (the lung),” Hai said.
First, the chemo appears to send signals to increase the number of molecular doors through which the cancer cells can escape from the primary tumor into the bloodstream, freeing them to travel to other organs, the researchers found.
“I think it’s an active process – a biological change in which the cancer cells are beckoned to escape into the blood — rather than a passive process in which the cancer cells get into the bloodstream because of leaky vessels,” said Hai, a member of The Ohio State University Comprehensive Cancer Center.
This finding is bolstered by another recent study conducted at the Albert Einstein College of Medicine and published in Science Translational Medicine, which showed a similar result using imaging techniques to observe the tumor in mice, Hai said.
Second, theOhio State researchers found that, beyond aiding cancer cell escape, paclitaxel creates a cascade of events that makes the tissue environment in the lung fertile ground for circulating cancer cells.
“There are signals that help cancer cells enter the lungs and set up shop, that make the environment more immunologically tolerant to cancer cells,” Hai said.
A molecular-level understanding of why chemotherapy sometimes increases risk of metastatic cancer is in the early stages, Hai said.
She said it’s important to recognize that the cancer cells in the study’s mouse model are very aggressive and that it would be interesting to test whether paclitaxel also enhances the escape of cancer cells at earlier stages in cancer progression.
Hai cautioned that much more work is required before extrapolating the findings in mice to human cancer treatment.
“At this point, what our study and the recent literature on chemotherapy taught us is that it is prudent to keep our mind open, realizing that chemo can help treat cancer, but at the same time may increase the possibility of the spread of that cancer,” she said.
What set their study apart from other research in this area is the identification of the stress gene Atf3. They showed that paclitaxel — a stressor — exerts its pro-cancer effect at least in part by turning on Atf3.
“It’s possible there could be a treatment given in conjunction with the chemo that would inhibit this problem by dampening the effect of the stress gene Atf3,” Hai said.
And that will be a focus of Hai’s work in this area going forward, she said.
The U.S. Department of Defense supported this study.
Other Ohio State researchers who worked on the study were Yi Seok Chang, Swati Jalgaonkar and Justin Middleton.