lymphoplasmacytic_lymphoma%eb%b2%88%ec%97%ad%eb%b3%b8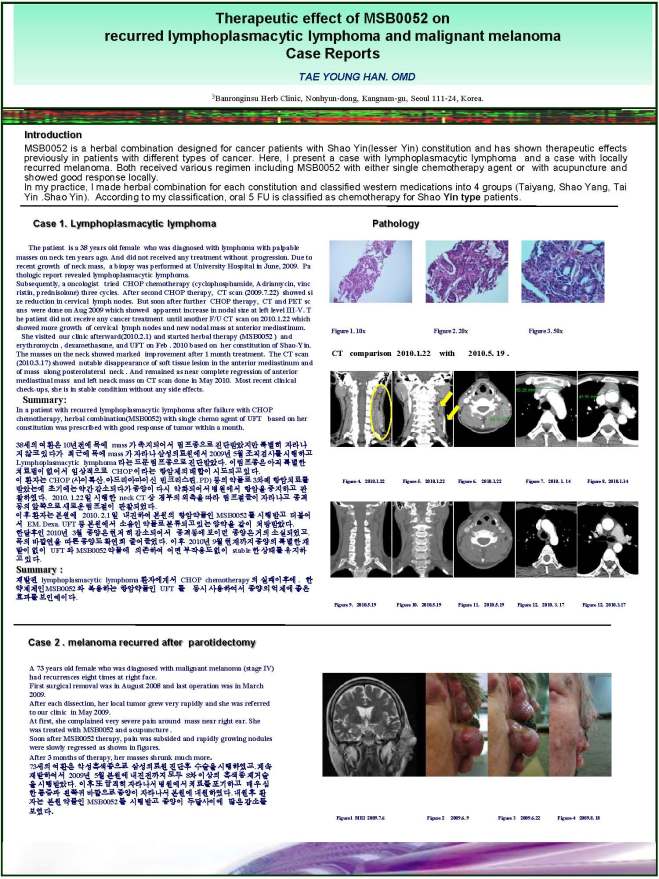
림프종은 양방에서 비교적 완치가 높은 혈액암이지만 그 중에서 치료가 잘 안되거나 재발율이 높은 경우도 많다. 림프종이 걸리는 환자들은 대부분이 소음인과 태음인들인데 림프종은 종류가 매우 많아서 다 겪어보지 못하여서 감히 왈가왈부 할 수가 없지만 본원에서 경험하고 치료된 몇몇 경우를 보면양방항암제와 한방약물을 적절히 결합하여서 좋은 결과를 볼 수가 있다.
여기서 소개하는 환자는 38세의 여환으로 10년 전에 목에 mass가 촉지되어서 림프종으로 진단받았지만 특별히 자라나지 않고 있다가 최근에 목에 mass가 자라나 삼성의료원에서 2009년 5월 조직검사를 시행하고 Lymphoplasmacytic lymphoma 라는 드문 림프종으로 진단받았다. 이 림프종은 아직 특별한 치료법이 없어서 임상적으로 CHOP 이라는 항암제의 배합이 시도되고 있다.
이 환자는 CHOP (사이톡산, 아드리아마이신 빈크리스틴, PD) 등의 약물로 3차례 항암치료를 받았는데 초기에는 약간 감소되다가 종양이 다시 악화되어서 병원에서 항암을 중지하고 관찰하였다. 2010년 1월 22 일 시행한 neck CT 상 경부의 외측을 따라 림프절들이 자라나고 종격동의 앞쪽으로 새로운 림프절이 관찰되었다.
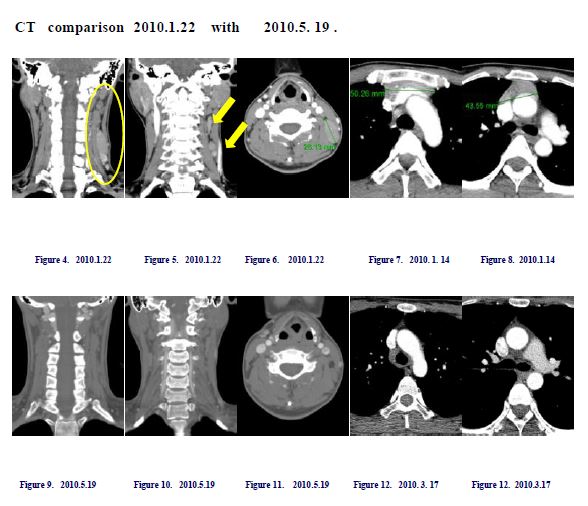
-위의 사진에 노란 원과 화살표가 경부에 재발되었던 림프절이고 오른쪽 사진에 보이는 선으로 그어진 부분이 종격동의 흉골 부위에 생긴 림프절로 당시 재발하자 주치의가 별로 약이 반응을 안 하고 특별히 이 병에 연구가 잘 안 되어 있어서 지켜보고 관찰해 보자고 하자 환자가 본원을 내원한 경우로
이후 환자는 본원에 2010년 2월 1일 내진하여 본원의 항암약물인 MSB0052 를 시행받고 더불어서 EM. Dexa. UFT 등 본원에서 소음인 약물로 분류되고 있는 양약을 같이 처방받았다.
한 달 후인 2010년 3월 종양은 현저히 감소되어서 종격동에 보이던 종양은 거의 소실되었고, 목의 바깥연을 따른 종양도 확연히 줄어들었다. 이후 2010년 9월 현재까지 종양의 특별한 재발이 없이 UFT와 MSB0052 약물에 의존하여 어떤 부작용도 없이 stable 한 상태를 유지하고 있다.
Summary :
재발된 lymphoplasmacytic lymphoma 환자에게서 CHOP chemotherapy의 실패 이후에, 한약제제인 MSB0052 와 복용하는 항암약물인 UFT를 동시 사용하여서 종양의 억제에 좋은 사례로 청풍 국제 학술 대회에 발표를 한 경우이다.
이 환자는 2010년부터 2014년 10월까지 한방약물과 항암제 복용을 병용하여 종양이 거의 없어진 상태로 완전관해로 삼성의료원에서 판명받고 한방치료를 종료하였다.
이후에 환자가 그간 식이요법으로 먹어 보지 못하였던 체질 금기 식품인 돼지고기 등의 육류와 양인들의 식품을 2년간 마음 놓고 먹었는데 최근에 2016 년 9월에 다시금 이전에 촉지되었던 경부 임파절이 조금 커지는 듯하여서 내원하여 치료를 다시 시작하고 있다.
림프종은 종류마다 너무 다른 치료율이나 예후의 차이를 보이지만 많은 경우 골수이식 등에 의존하는데 동종이식요법도 부작용이 많아 숙주편대 반응이 일어나서 고생하기도 하고 이식 후 초기에 부작용으로 사망율도 높은 편이다. 또한 T cell과 B cell이 다르지만 재발율이 높은 경우도 많은데 이lymphoplasmacytic lymphoma는 매우 드문 경우로 본원에서 한 case 를 만나 보았고 치료가 잘 되어서 관해되었으나 역시 식이요법이 그간 따라주지 않다가 2 년여 만에 다시금 재발한 경우로 역시 치료 이후에 확연히 줄어드는 효과를 보이고 있다. 따라서 암환자들은 치료 후에도 체질식을 지키는 것이 매우 중요하다.
참고로 wikipedia 에 실린 이 암에 관한 자료를 번역해서 실어보겠다.
왈덴스트롬의 마크로글로부린혈증으로도 불리우는 림포프라스마사이틱 림프종은 B cell에 영향을 주는 림프종이다. 이에 관여하는 항원은 -면역글로부린M(IgM)으로 이는 비교적 완만하게 자라고 퍼지는 종양이다. 이는 림프구가 증식하는 질환으로 서서히 자라는 비호지킨림프종에 속한다. 이 질환은 스웨덴의 종양학자인 Jan.G . Waldenstrom이 1944년 처음으로 발견함으로써 이렇게 명명하게 된다. 또한 다른 림프종과 마찬가지로 이는 제어되지 않는 B cell의 증가가 특징이다. 이는 골수와 림프절에서 형성되는 백혈구의 하나로서 B cell의 증식이 결국 적혈구의 생산을 방해하므로 빈혈을 초래하게 된다.또한 이 질환의 특징은 B cell이 과대한 양의 면역글로부린을 생산하고 혈액을 진하게 한다. 그리하여 이를 위한 특별한 조치가 필요하다. 이는 매우 드문 질환으로 현재 미국에서 한 해 동안 1500 case가 보고된다. 이 종양은 불치의 병이지만, 어느 정도 조치로 억제가 가능하다. 비교적 완만히 자라나는 특성때문에 많은 환자들이 일상 활동을 할 수가 있고, 치료가 필요할 때 완치되지는 않지만 몇 해 동안은 증상 없이 불완전 관해가 되는 경우가 있다.
1944년에 왈덴스트롬이란 스웨덴 의사가 두 환자가 코와 입에서 출혈이 있으면서 빈혈이 나타나고, 혈액 중의 응고성분인 fibrinogen이 매우 감소 하면서 림프절이 증가된 것을 발견하였다. 또한 골수에서 변형된 종양화된 혈장세포와 마크로 글로부린이라는 무거운 비중의 단백질이 매우 증가됨으로써 혈액의 점도가 높아진 것을 알게 되었다. 한동안 이 질환은 단크론글로부린혈증과 plasmacytoid lymphocytes 가 골수와 다른 장기를 침범하므로 다발성 골수종과 연관된 것으로 생각되었다. WHO 분류체계에서는 이를 비호지킨스 림프종의 카테고리 하에 lymphoplasmacytic lymphomas로 분류하였다. 그리고 최근에는 이 질환에 관한 이해와 치료에 많은 진전이 있었다.
증상
증상은 쇠약감과 체중감소와 피로감과 함께 만성적인 코와 잇몸에서의 출혈 등이다. 말초 신경염도 10%의 환자에게서 보이고, 림프절종대와 비장종대 혹은 간종대가 30-40%의 환자에게 나타난다. 또한 시야가 흐려지고 두통도 나타나고 드물게는 혼수상태나 뇌경색 등도 보인다. 또한 이 질환의 중앙 생존값은 6.5 년이다.
Waldenström’s macroglobulinemia – Wikipedia 인용
Waldenström’s macroglobulinemia (WM), also known as lymphoplasmacytic lymphoma, is a type of cancer affecting B cells, a type of white blood cell. The main attributing antibody is immunoglobulin M (IgM). WM is an “indolent lymphoma” (i.e., one that tends to grow and spread slowly). It is a type of lymphoproliferative disease, which shares clinical characteristics with the indolent non-Hodgkin lymphomas.[1]
The disease, named after the Swedish oncologist Jan G. Waldenström, was first identified in 1944. As with other lymphomas, it is characterized by an uncontrolled increase of B cells: white blood cells formed in the bone marrow and lymph nodes. The proliferation of B cells interferes with the production of red blood cells, resulting in anemia. A unique characteristic of the disease is that the B cells produce excess amounts of immunoglobulin, thickening the blood and requiring additional treatment. WM is a rare disease, with only about 1,500 cases per year in the United States. While the disease is incurable, it is treatable. Because of its indolent nature, many patients are able to lead active lives, and when treatment is required, may experience years of symptom-free remission.[2]
History and classification[edit]
WM was first described by Jan G. Waldenström (1906–1996) in 1944 in two patients with bleeding from the nose and mouth, anemia, decreased levels of fibrinogen in the blood (hypofibrinogenemia), swollen lymph nodes, neoplastic plasma cells in bone marrow, and increased viscosity of the blood due to increased levels of a class of heavy proteins called macroglobulins.[3]
For a time, WM was considered to be related to multiple myeloma because of the presence of monoclonal gammopathy and infiltration of the bone marrow and other organs by plasmacytoid lymphocytes. The new World Health Organization (WHO) classification, however, places WM under the category of lymphoplasmacytic lymphomas, itself a subcategory of the indolent (low-grade) non-Hodgkin lymphomas.[4] In recent years, there have been significant advances in the understanding and treatment of WM.[5]
Signs and symptoms[edit]
Signs and symptoms of WM include weakness, fatigue, weight loss, and chronic oozing of blood from the nose and gums.[6] Peripheral neuropathy occurs in 10% of patients. Lymphadenopathy and enlargement of the spleen, and/or liver are present in 30–40% of cases.[7] Other possible signs and symptoms include blurring or loss of vision, headache, and (rarely) stroke or coma.
Causes[edit]
Waldenström’s macroglobulinemia is characterized by an uncontrolled clonal proliferation of terminally differentiated B lymphocytes. The most common causes are a somatic mutation in MYD88 (90% of patients) and a somatic mutation in CXCR4 (27% of patients).[8] An association has been demonstrated with the locus 6p21.3 on chromosome 6.[9] There is a two- to threefold increased risk of WM in people with a personal history of autoimmune diseases with autoantibodies, and a particularly elevated risk associated with liver inflammation, human immunodeficiency virus, and rickettsiosis.[10]
There are genetic factors, with first-degree relatives of WM patients shown to have a highly increased risk of also contracting the disease.[11] There is also evidence to suggest that environmental factors, including exposure to farming, pesticides, wood dust, and organic solvents, may influence the development of WM.[12]
Prognosis[edit]
Current medical treatments result in survival of some longer than 10 years; in part this is because better diagnostic testing means early diagnosis and treatments. Older diagnosis and treatments resulted in published reports of median survival of approximately 5 years from time of diagnosis.[1] Currently, median survival is 6.5 years.[48] In rare instances, WM progresses to multiple myeloma.[49]
The International Prognostic Scoring System for Waldenström’s Macroglobulinemia (IPSSWM) is a predictive model to characterise long-term outcomes.[50][51] According to the model, factors predicting reduced survival[52] are:
- Age > 65 years
- Hemoglobin ≤ 11.5 g/dL
- Platelet count ≤ 100×109/L
- B2-microglobulin > 3 mg/L
- Serum monoclonal protein concentration > 70 g/L
The risk categories are:
- Low: ≤ 1 adverse variable except age
- Intermediate: 2 adverse characteristics or age > 65 years
- High: > 2 adverse characteristics
Five-year survival rates for these categories are 87%, 68% and 36%, respectively.[53]
The IPSSWM has been shown to be reliable.[54] It is also applicable to patients on a rituximab-based treatment regimen.[53] An additional predictive factor is elevated serum lactate dehydrogenase (LDH).[55]
Treatment[edit]
There is no single accepted treatment for WM.[56] There is marked variation in clinical outcome due to gaps in knowledge of the disease’s molecular basis. Objective response rates are high (> 80%) but complete response rates are low (0–15%).[5] Recently, Yang et al. showed that the MYD88 L265P mutation induced activation of Bruton’s tyrosine kinase, the target of the drug ibrutinib. Among previously treated patients, ibrutinib induced responses in 91% of patients, and at 2 years 69% of patients had no progression of disease and 95% were alive (Treon et al., New England Journal of Medicine 2015). Based on this study, the Food and Drug Administration approved ibrutinib for use in WM in 2015.[57]
There are different treatment flowcharts: Treon[58] and mSMART.[59]
WM patients are at higher risk of developing second cancers than the general population, but it is not yet clear whether treatments are contributory.[60]
