췌장암에 대한 사상의학적 치료를 설명하기 전에 먼저 췌장암에 대한 논문을 통하여서 생존률 등을 고려해 보려고 한다. 나의 사상의학적인 방법은 한방과 양방약물을 결합치료하는 것이 주된 방법이며 체질에 따른 항암제의 고려가 우선이 된다. 2009년도 발표된 “사상의학을 기반으로 한 동서의학 암 진료 협진 사례 분석”은 보건복지 가족부의 위탁연구로 아주대학교 산학협력단이 주관 연구기관이었다. 복지부에서 특별 자금을 주어서 아주대의 전미선 교수 주관 아래 본원의 사상체질에 의한 한방치료 요법이 암에 어떠한 결과를 가져오는지와 더불어서 양약을 분류하여서 말기 환자들에게 사용하는 방법이 유효성이 있는지를 밝혀보자 하는 것이었다.
주관 연구책임자는 아주대 방사선종양학과의 전미선 교수였고, 아주대학교 혈액종양학과 이현우 교수, 아주대학교 병리학과 주희재 교수 등이 관여하였고 아주대학교에서 임상간호사를 본원 반룡인수한의원에 파견하여서 1년간 나의 진료에 참관하면서 내 clinic의 항암치료 결과를 보고하고 정리하고 통계를 내었다.
당시 연구 목표를 그대로 옮겨 보면-
- 사상의학적으로 체질을 구분하여 항암제와 한약을 선택적으로 결합하여 말기 암환자를 성공적으로 치료한 사례를 발굴하고 의학적으로 분석함
- 사상의학을 기반으로 하는 동서의학 협진의 임상연구 모델 제시
연구내용은 말기 췌장암 담도 및 담낭암 폐암 환자 68명의 의무기록을 리뷰 정리
- 드문 소아암 환자의 사례 정리
- 각 암종별 치료경과 정리 및 생존률 분석
- 임상연구 모델 제시
등이었다. 실제로는 300 여 case를 정리하였지만 본원에 오는 환자들은 대부분이 말기 중의 말기에 오다 보니까 기록이 결여된 경우가 있고 개인 의원의 한계때문에 정확하게 혈액학적이나 주기적인 방사선학적인 검사를 갖추고 있는 경우만 보다 보니까, 실제로 논문에 넣기에 적합한 자격 요건을 갖추고 있는 68 case밖에 통계에 넣지 못하였다. 하지만 나머지 자료들도 모두 자료화 하여서 그 치료과정과 결과를 보고하였다.
연구결과는
- 췌장암 4기 및 진행성 암환자들의 중앙생존값은 한방치료 기간에 따라 13개월(6개월 미만 치료기간)과 20개월(6개월 이상의 치료기간)로 최신 항암치료를 사용한 임상연구 결과보다 나은 결과를 보였음.
- 담도 담낭암 4기 및 진행성 암환자들의 중앙생존값은 한방치료 기간에 따라 6개월 미만 치료기간의 환자군은 5개월로 발표된 임상연구결과와 유사하였고 6개월 이상 치료기간 환자군은 20개월로 발표된 임상결과보다 나은 결과였다. 단 3명의 대상자인 제한점이 있음.
- 사상의학을 기반으로 한방치료와 일부 암 치료를 병용함으로써 부작용은 적게, 종양의 감소 또는 유지하는 사례를 확인할 수 있었음.
- 소아암의 경우 수차례의 암 치료 실패 후 한방치료로 종양의 감소 효과를 보여준 사례를 보여줌.
- 기타 암환자에서 사상의학을 응용한 치료로 부작용 호전 및 증상완화 등의 사례 보고함.
- 한방과 항암제 치료를 병용한 경우도 간 독성을 보고한 경우는 없었음.
제언
- 양한방 협진을 위한 체계화된 의무기록 양식이 필수임
- 양한방 협진시 영상검사 등 추적관찰을 위한 자료가 필수임
- 실시간 양한방 협진 진료를 위한 원격진료가 필요함.
- 임상연구 모델 – 말기 췌장암 담도 및 담낭암 환자들에서 일반정통 암 치료와 한방 병용치료와 비교연구 / 항암치료에 실패한 소아암 환자의 양한방 협진으로 종양억제 효과 확인을 위한 임상연구/ 말기암 환자의 완화 의료를 위한 한방이 효용성 확인을 위한 임상연구
기대성과
- 말기암 환자에서 부작용을 최소화 및 증상 감소. 일상생활의 유지 등 삶의 질 향샹 효과를 위한 사상의학을 기반으로 하는 양한방 협진 가능성 확인
- 소아암 환자에서의 사상의학을 응용한 양한방 협진의 유용성 확인
- 양한방 협진 진료용 기록지 개발
위는 복지부위탁연구 결과서에 대한 요약을 그대로 옮겨 적은 것이다.
위에서 이야기되듯이 나의 의원에 오는 암환자들은 거의 말기 중의 말기라 더 이상 양방방법을 시행하지 못하고 호스피스로 가라고 하면 그제서야 오던지, 아니면 처음 발견했을 때 너무 상태가 나쁜 4기 환자들 뿐이다. 그래서 CT 등의 검사도 권유하기 부담스럽고 특히 간담도계 종양인 췌장 담도 담낭암은 조영제가 미치는 영향도 적지 않아서 검사를 건너뛰기도 하다 보니 딱 맟추어서 병원을 다니면서 병용치료를 한 경우가 아니면 자료화 하기가 힘들었다. 그래서 많은 사례를 정리하지 못하였다. 하지만 2009년도의 연구이고 본고에서는 이러한 한계를 넘어서 비록 자료가 미비하고 통계에 넣기가 어려운 환자의 경우라도 말기 환자들이 한방치료로 어떻게 유지가 되었는지를 보여주기 위하여서 좀더 많은 case를 넣어보려고 한다.
당시 연구에 대상으로 넣은 췌장암 환자는 총 62명이었는데 여러 가지 이유로 배제하다 보니 결국 16명이 추려지었다.
췌장암 치료결과 논문고찰을 그대로 옮긴다.

췌장암은 미국의 소화기 암 중 2번째로 많은 암이며 성인에서 암 사망원인 중 4번째로 많다. 국내에서도 질병 양상의 서구화로 발생빈도가 70년 동안 3배 이상 증가하였고 향후에는 발생빈도가 현저히 증가하여 2003년에서 2005년 사이 연 평균 3443건으로 전체 암 발생의 2.6%로 9위를 차지하며 국내 암 관련 사망에서 5위를 차지한다. 췌장암은 가장 예후가 불량한 암 중 하나로 2년 생존율이 10% 내외이며 병원 방문 당시 이미 병이 진행되어서 수술을 시행할 수 없는 경우가 90%에 달한다.
췌장암에서 완치를 위한 치료법은 근치적 절제술이나 진단 당시 이미 수술을 시행할 수 없을 정도로 진행된 경우가 대부분이며, 수술을 시행하더라도 국소 재발율은 50-80%이며,전신전이의 경우 75%로 수술로도 완치가 어려운 암이다. 전이된 췌장암의 경우 현재의 항암제로 치료반응은 있는 항암제가 반응율은 6-13%이고 중앙생존기간이 4.9-9개월로 매우 예후가 좋지 않다. 췌장암에서 흔히 사용하는 gemcitabine과 tarceva 병합 요법과 gemcitabine 단독요법의 3상 비교연구에서 중앙생존기간은 각각 6.24개월과 5.91개월이었으며, 1년 생존율은 각각 23%, 18 %였다.
위에서 이야기되듯이 처음 발견할 때부터 초음파로 쉽게 보이지 않기 때문에 초기에는 소화 불량 정도로 여기다가 계속 등짝이 아파서 초음파를 해 보아도 놓지는 경우가 많다. 급기야 병이 진행이 되어서 확연히 아플 때는 이미 많이 진행이된 상태이다. 한마디로 병기를 따지지 않고 중앙생존기간이 6개월 남짓한 게 췌장암이다.
그러나 수술이 가능한 경우는 이와 다른 보고가 있다.
Actual long-term outcome of T1 and T2 pancreatic ductal adenocarcinoma after surgical resection.
Han SH1, Heo JS2, Choi SH1, Choi DW1, Han IW1, Han S1, You YH1.
Abstract
BACKGROUND:
The prognosis for patients with pancreatic cancer is extremely poor. The diagnosis of pancreatic ductal adenocarcinoma at an early stage is uncommon. The purpose of this study was to analyze the clinicopathological characteristics of patients with pathologically proven pancreatic ductal adenocarcinoma following surgical resection and their actual 5 year survival rates, especially for those with T1 and T2 early stage cancer.
췌장암 환자의 예후는 매우 불량하다. 췌장의 ductal adenocarcinoma의 초기 병기인 환자는 매우 드물다. 이 논문의 목적은 병리학적으로 증명된 췌장의 ductal adenocarcioma 환자의 임상병리학적인 특성을 분석하고 수술에 따른 5년 생존율을 측정하는 것으로 특별히 T1 T2의 초기 병기의 환자군을 대상으로 한다.
METHODS:
Retrospective analysis was performed for 433 patients with pancreatic ductal adenocarcinoma who underwent resection at Samsung medical center between May 1995 and December 2010. The actual 5 year survival rates and prognostic factors were analyzed.
회고적인 분석이 총 433명의 췌장 췌관선세포암을 진단받고 삼성의료원에서 1995년 5월부터 2010년 12월까지 기간 동안 절제술을 받았던 환자군을 대상으로 하였다. 실제적인 5년 생존율과 예후에 대한 요인이 분석 되었다.
여기서 환자분들의 이해를 돕기 위해서 췌장암의 병기에 대한 설명을 잠시 보충해 보겠다.

RESULTS:
Multivariate analysis showed that positive resection margin, poor differentiation, large tumor size, large amount of blood loss, and T3/T4 were independent prognostic factors on overall survival. The median survival for T1/T2 stage was 71.7 months compared to 16.1 months for those with T3/T4 stage. The actual 5 year survival rates for T1/T2 and T3/T4 stages were 66.7% and 18.4%, respectively.
다양한 분석법이 절제선에서 종양이 침범여부나 악성분화도 커다란 종양크기, 많은 양의 혈액 소실, 그리고 T3/ T4 (종양이 췌장 바깥으로 퍼져서 상장간동맥이나 복강동맥을 침범하거나 혹은 하지 않은 경우) 등이 중요한 생존율에 영향을 미치는 요인이었다. T1/T2 stage(종양이 췌장 내에만 머물 때)의 중앙생존기간은 71.7개월 (약 6년)이었고 종양이 췌장 바깥으로 퍼져 있을 때는(T3/T4 stage)에서는 16.1개월 이었다. 실제적인 5년 생존율은 T1/T2는 66.7%였고 T3/T4에서는 18.4%였다.
CONCLUSIONS:
T stage is one of the strongest independent prognostic factor for overall survival of patients with pancreatic cancer. T1/T2 pancreatic ductal adenocarcinoma showed good survival outcome. Therefore, additional efforts are needed to improve the screening for early detection.
결론적으로 T stage는 가장 강력한 환자들의 생존율에 영향을 주는 요인이라고 본다. 그러므로 종양을 일찍 발견하는 것이 좋은 생존의 결과를 가져 오게 될 것이다.
이 논문에 의하면 췌장암 환자도 매우 낙관적인 생각을 할 수 있다. 아마도 삼성의료원에서 치료받은 환자들의 경우에는 췌장암이라도 절제만 할 수 있고 췌장 바깥으로 퍼지지 않은 경우는 거의 6 년을 쉽게 살 수 있다는 이야기가 된다. 리고 66%의 환자는 무난히 5년을 넘기게 되고 34% 정도의 환자가 5년 안에 죽는다는 이야기이다.
이는 아주대에서 본 예후와는 너무도 다르다. 물론 아주대의 경우는 수술을 하였던지 안하였던지를 따지지 않은 최신의 결과들을 집합한 것이다.
이와 다른 결과를 보여주는 미국에서 연구된 논문을 하나 소개해 보겠다.
Pancreatic Cancer: Diagnosis and Management
Am Fam Physician. 2006 Feb 1;73(3):485-492.
Although only 32,000 new cases of adenocarcinoma of the pancreas occur in the United States each year, it is the fourth leading cause of cancer deaths in this country. The overall five-year survival rate is 4 percent, and localized, resectable disease has only a 17 percent survival rate. Risk factors include smoking, certain familial cancer syndromes, and familial chronic pancreatitis. The link between risk of pancreatic cancer and other factors (e.g., diabetes, obesity) is less clear. Most patients present with obstructive jaundice caused by compression of the bile duct in the head of the pancreas. Epigastric or back pain, vague abdominal symptoms, and weight loss also are characteristic of pancreatic cancer. More than one half of cases have distant metastasis at diagnosis. Computed tomography is the most useful diagnostic and staging tool. Ultrasonography, magnetic resonance imaging, and endoscopic retrograde cholangiopancreatography may provide additional information. The majority of tumors are not surgically resectable because of metastasis and invasion of the major vessels posterior to the pancreas. Resectable tumors are treated with the Whipple procedure or the pylorus-preserving Whipple procedure. Adjuvant fluorouracil-based chemotherapy may prolong survival. For nonresectable tumors, chemotherapy with gemcitabine prolongs survival. Other agents are being studied. Radiation combined with chemotherapy has slowed progression in locally advanced cancers. Throughout the illness and during end-of-life care, patients need comprehensive symptom control.
The American Cancer Society estimated that 31,860 Americans would be diagnosed with pancreatic cancer in 2004, and that 31,270 would die from the disease.1 Pancreatic cancer accounts for only 2 percent of all new cancers in the United States, but it is the fourth leading cause of cancer deaths. At the time of diagnosis, more than one half of pancreatic cancers have metastasized, and only 8 percent are localized. The overall five-year survival rate is 4 percent. Localized cancers have a 17 percent survival rate. Survival rates have not improved during the past 25 years.1
Pancreatic cancer rarely occurs in persons younger than 50 years, and the risk increases with age. The incidence of pancreatic cancer is declining slowly in white men, but it is increasing in other groups, possibly because of changes in smoking patterns. Women account for 57 percent of new cases.1 Smoking,2 diabetes,3 and obesity4 increase risk. A link between alcohol or coffee consumption and pancreatic cancer has not been verified.5 Physical activity; high fruit and vegetable intake6; and, possibly, nonsteroidal anti-inflammatory drugs reduce the risk.7 Up to 10 percent of patients report a family history of pancreatic cancer.8 Patients with rare familial cancer syndromes or hereditary chronic pancreatitis have a substantially increased risk.9 Research on overexpression of specific oncogenes10 and reduced activity of tumor suppressor genes may provide a better understanding of the pathogenesis of pancreatic cancer and lead the way to more effective screening tests.11,12
췌장 선암의 32,000 새로운 환자가 매년 미국에서 발생하지만, 이 나라에서 암 사망의 네 번째 주요 원인이다.전체 5년 생존율은 4%이고, 국소적인 종양 절제는 17%의 생존율을 갖는다. 위험 인자는 흡연, 특정 가족성 암 증후군 및 가족성 만성췌장염을 포함한다. 췌장암 및 다른 요인인(예를 들면, 당뇨병, 비만)과의 관계는 덜 명확하다. 췌장의 두부에 발생한 경우에서 담관의 눌림으로 인한 담즙억제로 오는 폐쇄성 황달에 존재하는 대부분의 환자의 상복부 또는 허리 통증, 막연한 복부 증상, 체중 감소는 췌장암의 특징이다. 환자의 절반 이상은 진단시 원격 전이가 있다. 전산화 단층 촬영은 가장 유용한 진단 및 준비 도구이다. 초음파, 자기 공명 영상, 내시경 역행 췌담관 조영술 추가 정보를 제공할 수 있다. 종양의 대부분은 췌장 바깥으로 전이되고 주요 혈관들을 침범하므로 외과적 절제술이 불가능하다. 절제 가능한 경우에 종양은 위플 수술 또는 유문 보존 위플 수술을 하게 된다.
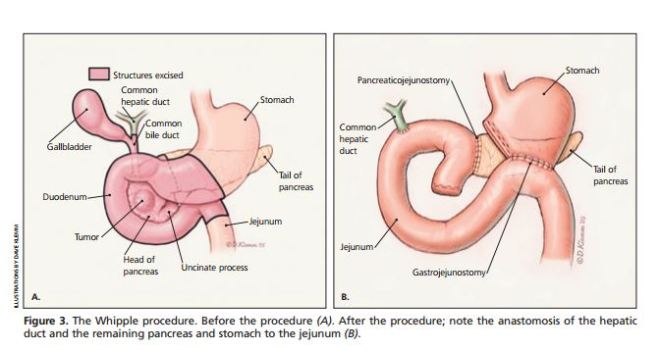
보조적으로 (5-Fu)프를로 우라실 기반 화학 요법은 생존을 연장할 수 있다. 수술 불가능한 종양의 경우, 젬시타빈을 기반으로 하는 화학요법은 생존을 연장시킬 수 있고 또 다른 약물들이 연구되고 있다. 화학요법과 함께 방사선치료는 국소 진행성 암의 진행을느리게 하지만 아픈 전 기간 동안 사망에 이르기까지 환자는 광범위한 증상을 위한 약물이나 여타의 방법으로 통증을 제어하고 담즙배설을 돕는 등의 한 증상 조절이 필요하다.
미국 암 협회는 2004년에 31,860 미국인이 췌장암으로 진단받고, 31270이 질병으로 사망 것이 될 것이라고 추정했다. 1췌장암이 미국에서 모든 새로운 암의 2 %를 차지하지만, 암 사망의 네 번째 주요 원인이다. 진단시, 췌장암의 절반 이상은 전이가 있고, 단지 8 %는 국소적으로 발생된다. 전체 5년 생존율은 4 %이다. 국소적으로 췌장에만 발생한 경우는 17 % 생존율을 갖는다. 생존율은 지난 25년 동안 개선되지 않았다.1
췌장암은 거의 오십 이하의 젊은 사람에서는 발생율이 적고 나이가 높을수록 위험은 증가한다. 췌장암의 빈도는 백인의 경우 천천히 감소되지만 다른 인종에서는 증가하고 있는데 아마도 흡연 패턴의 변화 때문일 것으로 추정된다. 여성도 새로운 발생하는 사례의 57퍼센트를 차지한다. 1 흡연, 2 당뇨병, 3 , 비만 4등은 췌장암을 증가시킬 수 있는 위험요인이지만, 알코올이나 커피 소비와 췌장암 사이의 연관성은 확인되지 않았다.(5) 운동, 과일과 야채 섭취 (6) 및, 아마도 비 스테로이드성 항염증 약물의 사용은 췌장암의 발생을 감소시킨다. 7 환자의 최대 10%가 췌장암의 가족력을 보고합니다. 8 희귀한 가족성 암 증후군 또는 유전 만성 췌장염 환자는 실질적 위험이 있다. (9) 특정 암 유전자의 과발현을 연구 10 종양 억제 유전자의 활성을 감소시킴으로써 췌장암의 병인에 대한 이해를 제공하는 보다 효과적인 선별 검사를 초래할 수 있다. (11) , (12)
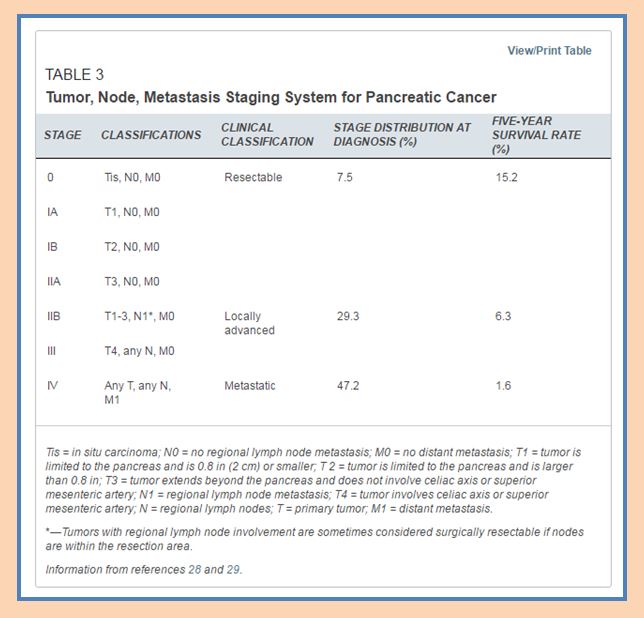
여기서는 Tis 즉 0기 췌장암의 수술이 가능한 경계성 종양 환자의 경우 5년 생존율이 15.2% 라고 보고 하고 있다. 가장 종양의 분화도가 낮은 T1s에서 수술이 가능했던 환자들도 5년 생존율이 15%밖에 안된다고 한 것은 한국의 논문과 너무도 심한 차이가 난다. 한국에서는 T3 T4 환자들의 5년 생존율이-수술로 처치를 한-18.4%였고 T1. T2의 환자는 5년 생존율은 66.7%이다. 이 논법으로 따지면 Tis 환자들은 아마도 70-80%가 5년 생존이 가능하다는 이야기이다.
췌장암 환자는 다 한국에 와서 치료받아야 한다는 결론이 된다. 우리보다도 의학 선진국인 미국에서 경계성 췌장암으로 수술 가능한 자가 5년 생존율이 15.2 %밖에 안되는 것에 비하면 삼성의료원의 치료방법이나 수술기술은 대단한 것이다.
한국에서 쓰여진 논문과 비슷한 시기의 환자를 분석한 영국 암 잡지(British journal Cancer)의 논문을 수록해 보겠다.
Overall survival and clinical characteristics of BRCA mutation carriers with stage I/II pancreatic cancer.
Golan T1,2, Sella T1,2, O’Reilly EM3,4, Katz MH5, Epelbaum R6,7, Kelsen DP3,4, Borgida A8, Maynard H3,4, Kindler H9, Friedmen E2,10, Javle M11, Gallinger S8.
Abstract
BACKGROUND:
BRCA1/BRCA2 germ line (GL) mutation carriers with pancreatic adenocarcinoma (PDAC) may have distinct outcomes. We recently described an apparent more favourable prognosis of surgically resected BRCA-associated PDAC patients in a single-arm, uncontrolled, retrospective study. However, the prognostic impact of GL BRCA1/2 mutations in surgically resected PDAC has not been compared with a matched control population.
METHODS:
A larger multi-centre, case-control retrospective analysis was performed. Cases were patients with surgically resected, BRCA1/2-associated PDAC from 2004 to 2013. Controls included surgically resected PDAC cases treated during the same time period that were either BRCA non-carriers, or had no family history of breast, ovarian or pancreatic cancers. Cases and controls were matched by: age at diagnosis (within ±5-year period) and institution. Demographics, clinical history, overall survival (OS) and disease-free survival (DFS) were abstracted from patient records. Statistical comparisons were assessed using χ2– and Fisher’s exact test, and median DFS/OS using Kaplan-Meier method and log-rank testing.
여기서 대상으로 하는 군은 오늘날 유방암이나 난소암에서 많이 거론되고 있는 BRCA1/2의 유전자와 연관된 췌장관 선암환자로서 수술이 가능했던 환자의 2004년부터 2013년까지의 분석결과이다. 이들의 대조군으로는 BRCA의 유전자를 가지고 있지 않거나 가계에서 유방암이나 난소암 또는 췌장암의 병력이 없는 군의 수술이 가능했던 환자를 대조군으로 삼았다. 여기의 결론을 보면 물론 T stage를 분류하지 않았지만 수술이 가능했다고 하면 거의가 T1 T2로 보이는데 대략 중앙생존값이 37-38개월이며 DFS (disease free survivol-재발의 증상이나 징후가 없는 질병에서 자유로웠던 기간)은 14.3-12개월로 보고된다.
RESULTS:
Twenty-five patients with BRCA1-(n=4) or BRCA2 (N=21)-associated resectable PDAC were identified. Mean age was 55.7 years (range, 34-78 years), 48% (n=12) were females and 76% (n=19) were Jewish. Cases were compared (1 : 2) with 49 resectable PDAC controls, and were balanced for age, ethnicity and other relevant clinical and pathological features. BRCA-associated PDAC patients received neoadjuvant, or adjuvant platinum-based treatment more frequently than controls (7 out of 8 vs 6 out of 14) and (7 out of 21 vs 3 out of 44), respectively. No significant difference in median OS (37.06 vs 38.77 months, P=0.838) and in DFS (14.3 vs 12.0 months, P=0.303) could be demonstrated between cases and controls. A trend to increased DFS was observed among BRCA-positive cases treated with neoadjuvant/adjuvant platinum-containing regimens (n=10) compared with similarly treated controls (n=7) (39.1 vs 12.4 months, P=0.255).
CONCLUSIONS:
In this retrospective analysis, the prognosis of surgically resectable BRCA-associated PDAC is no different than that of sporadic PDAC from the same institution. The role of platinum-based adjuvant therapy in this setting requires prospective investigation.British Journal of Cancer (2017) 0, advance online publication, 9 February 2017; doi:10.1038/bjc.2017.19
반면에 수술이 불가능한 환자에서 화학치료와 방사선치료가 병행되었던 경우의 통계를 연구한 논문을 소개하겠다. 이는 서울대학교 서경규 교수가 발표한 논문이다(-서울 특별시 종로구 대학로 101 서울대학교 의과대학 방사선 종양학 교실). 이 논문의 대상자는 144명인데 국립대인 서울대에서 1989년부터 2013년까지이니 전체가 25년간에 144명이니 1년에 5.76명밖에 통계를 넣지 못하였다는 이야기이다. 그나마 13개월이 중앙생존기간이다. 즉 서울대에서 1년에 모든 췌장암 환자를 방사선 치료를 시키지는 않겠지만 1년에 6명만 통계를 넣을 수 있었다는 이야기는 그만큼 많은 환자들이 통계에 넣을 수 없을 정도로 빨리 사망한다는 이야기도 역으로 성립할 수 있다.
Outcome Analysis of Chemoradiation in Unresectable Pancreatic Cancer Focusing on Treatment Sequencing Strategy.
Koh HK1, Chie EK2,3, Kim K4, Jang JY5, Kim SW5, Oh DY6, Im SA6, Bang YJ6, Ha SW7,3.
Author information
목표
Aim: To analyze the outcomes of patients with unresectable pancreatic cancer after chemoradiotherapy (CCRT), focusing on sequencing strategy. Patients and Methods: Data of 144 patients treated from January 1989 to December 2013 were retrospectively analyzed. Patients were divided into the scheduled group (N=27), salvage group (N=37) and upfront group (N=80) per CCRT and chemotherapy sequence. Results: With a median follow-up of 10.4 months (range=1.4-164.2), median overall survival (OS) was 13.5 months. Patients in the upfront group had inferior performance status and received a lower radiation dose (p=0.007 and p<0.001, respectively). Higher radiation dose (≥45 Gy) was the sole prognosticator related with improved survival in multivariate (p=0.001) analysis, whereas treatment sequence was not a significant prognostic factor (p=0.409). Conclusion: No difference was found among tested sequencing strategies that were all well-tolerated, despite skewed distribution for performance and radiation dose. An upfront approach may be a viable option for patients with limited performance to undergo more active systemic chemotherapy.
목표 : 절제 불가능한 췌장암 환자의 화 방사선요법 (CCRT) 후 결과를 분석하고 시퀀싱 전략에 초점을 맞춘다. 대상 및 방법 : 1989년 1월부터 2013년 12월까지 치료받은 144명의 환자를 후향적으로 분석 하였다. 환자들은 CCRT 및 화학 요법 순서에 따라 계획된 그룹(N = 27), 구조 그룹(N = 37) 및 선행 그룹 N = 80)으로 나뉘었다. 결과 : 중간 추적 관찰기간이 10.4개월(범위 = 1.4-164.2)이었던 경, 전체 생존기간 (중앙값)은 13.5개월이었다. 선행 그룹의 환자들은 수행 상태가 열등하고 방사선량을 낮게 받았다(각각 p = 0.007 및 p <0.001). 치료 방사선 량이 유의한 예후 인자(p = 0.409)는 아니었지만, 다변량(p = 0.001) 분석에서 생존율 향상과 관련하여 방사선 선량(45 Gy 이상)이 유일한 예후 인자였다. 결론 : 성능 및 방사선량에 대한 왜곡 분포에도 불구하고 잘 견딜 수 있는 테스트 된 시퀀싱 전략에는 차이가 없었습니다. 제한된 수행 능력을 가진 환자들이 보다 적극적인 전신 화학 요법을 시행 할 수 있는 가능한 방법이 선행 접근법일 수 있습니다. 성능과 방사선량에 대한 왜곡 분포에도 불구하고,제한된 수행 능력을 가진 환자들이 보다 적극적인 전신 화학 요법을 시행 할 수 있는 가능한 방법이 선행 접근법 일 수 있습니다. 성능과 방사선량에 대한 왜곡 분포에도 불구하고, 제한된 수행 능력을 가진 환자들이 보다 적극적인 전신 화학요법을 시행 할 수 있는 가능한 방법이 선행 접근법일 수 있습니다.
Abstract
AIM:
To analyze the outcomes of patients with unresectable pancreatic cancer after chemoradiotherapy (CCRT), focusing on sequencing strategy.
PATIENTS AND METHODS:
Data of 144 patients treated from January 1989 to December 2013 were retrospectively analyzed. Patients were divided into the scheduled group (N=27), salvage group (N=37) and upfront group (N=80) per CCRT and chemotherapy sequence.
이 논문은 1989년 1월부터 2013년 12월까지의 144명에 대한 분석으로 크게 이야기하면 대략 중앙생존값이 13.5개월이었다.
RESULTS:
With a median follow-up of 10.4 months (range=1.4-164.2), median overall survival (OS) was 13.5 months. Patients in the upfront group had inferior performance status and received a lower radiation dose (p=0.007 and p<0.001, respectively). Higher radiation dose (≥45 Gy) was the sole prognosticator related with improved survival in multivariate (p=0.001) analysis, whereas treatment sequence was not a significant prognostic factor (p=0.409).
CONCLUSION:
No difference was found among tested sequencing strategies that were all well-tolerated, despite skewed distribution for performance and radiation dose. An upfront approach may be a viable option for patients with limited performance to undergo more active systemic chemotherapy.
Copyright© 2016 International Institute of Anticancer Research (Dr. John G. Delinassios), All rights reserved.
위에서 각기 다른 관점에서 연구를 하였기에 생존율이나 중앙생존값이 매우 다르게 표현된다. 그러면 최근에 American cancer society에서 발표한 생존율에 관한 자료를 살펴보겠다. 이 자료에 의하면 췌장의 신경내분비 종양으로 수술을 받은 경우에는 생존율이 비교적 높지만 일반적으로 우리가 생각하는 췌장암의 5년 생존율은 1기A가 14%, 1기B 가 12%, 2기A 가 7%, 2기B가 5%, 3기는 3%, 4기는 1% 로 췌장암 4기 환자의 5년 생존율은 100명 중에 1명으로 거의 전무하다는 이야기이다.
https://www.cancer.org/cancer/pancreatic-cancer/detection-diagnosis-staging/survival-rates.html
혹시라도 원본을 보고 싶고, 영어나 의학용어에 익숙하지 못한 분들은 위의 주소를 크릭한 다음에 마우스의 우측을 크릭하면 한국어로 번역이 나온다. 매우 정확하게 번역이 잘되었으므로 이를 참조하시길 바라고 여기서는 이 자료를 그대로 소개해 보겠다. 또한 한국어 번역이 안 나온다면 이 주소를 구글로 띄워서 마우스 크릭을 하면 한국어 번역이 매우 깔끔하게 되어 있다. 여기서는 이 번역을 약간만 수정하여서 소개하여 보겠다.
What is a 5-year survival rate?
Statistics on the outlook for a certain type and stage of cancer are often given as 5-year survival rates, but many people live longer – often much longer – than 5 years. The 5-year survival rate is the percentage of people who live at least 5 years after being diagnosed with cancer. For example, a 5-year survival rate of 70% means that an estimated 70 out of 100 people who have that cancer are still alive 5 years after being diagnosed. Keep in mind, however, that many of these people live much longer than 5 years after diagnosis.
But remember, the 5-year relative survival rates are estimates – your outlook can vary based on a number of factors specific to you.
특정 유형 및 암 단계에 대한 전망에 대한 통계는 종종 5년 생존율로 주어지지만, 많은 사람들은 5년보다 오래 – 혹은 훨씬 더 오래 사는 경우가 많습니다. 5 년 생존율은 암 진단 후 최소 5년 동안 살고 있는 사람들의 비율입니다. 예를 들어, 5 년 생존율이 70 %라는 것은 암을 앓고 있는 100명 중 70명이 추정 진단을받은 지 5 년 후에도 살아 있다는 것을 의미합니다. 그러나 이 사람들 중 상당수는 진단 후 5년 이상 오래 산다는 것을 명심하십시오.
그러나 5년 상대 생존율은 추정치입니다. 귀하의 전망은 귀하에게 특정한 여러 요소에 따라 달라질 수 있습니다.
Cancer survival rates don’t tell the whole story
Survival rates are often based on previous outcomes of large numbers of people who had the disease, but they can’t predict what will happen in any particular person’s case. There are a number of limitations to remember:
- The numbers below are among the most current available. But to get 5-year survival rates, doctors have to look at people who were treated at least 5 years ago. As treatments are improving over time, people who are now being diagnosed with pancreatic cancer may have a better outlook than these statistics show.
- These statistics are based on the stage of the cancer when it was first diagnosed. They do not apply to cancers that later come back or spread, for example.
- The outlook for people with pancreatic cancer varies by the stage (extent) of the cancer – in general, the survival rates are higher for people with earlier stage cancers. But many other factors can affect a person’s outlook, such as age and overall health, and how well the cancer responds to treatment. The outlook for each person is specific to their circumstances.
Your doctor can tell you how these numbers may apply to you, as he or she is familiar with your particular situation.
생존율은 종종 질병을 앓고 있는 많은 사람들의 이전 결과를 기반으로 하지만 특정 사람의 경우 어떤 일이 발생할 것인지 예측할 수는 없습니다. 기억해야 할 몇 가지 제한 사항이 있습니다.
- 아래의 숫자는 가장 최신의 것입니다. 그러나 5년 생존율을 얻으려면 의사가 적어도 5년 전에 치료를 받은 사람들을 봐야합니다. 치료법이 시간이 지남에 따라 개선됨에 따라 현재 췌장암으로 진단 받고 있는 사람들은 이러한 통계보다 더 나은 전망을 보일 수 있습니다.
- 이 통계는 암이 처음 진단되었을 때 암의 단계를 기반으로 합니다. 나중에 예를 들어 다시 확산되거나 확산되는 암에는 적용되지 않습니다.
- 췌장암 환자의 전망은 암의 단계 (범위)에 따라 다릅니다. 일반적으로 초기 암 환자의 생존율은 더 높습니다. 그러나 나이와 전반적인 건강 상태, 그리고 암이 치료에 얼마나 잘 반응하는지 등의 다른 요인들이 사람의 시력에 영향을 미칠 수 있습니다. 각 사람에 대한 전망은 상황에 따라 다릅니다.
의사는 특정 상황에 익숙하므로이 번호가 어떻게 적용될 수 있는지 알려줄 수 있습니다.
Survival rates for exocrine pancreatic cancer
The numbers below come from the National Cancer Data Base and are based on people diagnosed with exocrine pancreatic cancer between 1992 and 1998. In general, people who can be treated with surgery tend to live longer than those not treated with surgery.
- The 5-year survival rate for people with stage IA pancreatic cancer is about 14%. For stage IB cancer, the 5-year survival rate is about 12%.
- For stage IIA pancreatic cancer, the 5-year survival rate is about 7%. For stage IIB cancer, the 5-year survival rate is about 5%.
- The 5-year survival rate for stage III pancreatic cancer is about 3%.
- Stage IV pancreatic cancer has a 5-year survival rate of about 1%. Still, there are often treatment options available for people with this stage of cancer.
Remember, these survival rates are only estimates – they can’t predict what will happen to any individual person. We understand that these statistics can be confusing and may lead you to have more questions. Talk to your doctor to better understand your specific situation.
외분비 췌장암의 생존율
아래 수치는 National Cancer Data Base에서 얻은 것이며 1992년과 1998년 사이에 외분비 학상 췌장암으로 진단받은 사람들을 기준으로 합니다. 일반적으로 수술을 받을 수 있는 사람들은 수술하지 않은 사람들보다 오래 사는 경향이 있습니다.
- 병기 1A 췌장암 환자의 5년 생존율은 약 14%입니다.
- II기 IB 암의 경우 5년 생존율은 약 12%입니다.
- IIA기 췌장암의 5년 생존율은 약 7%입니다.
- IIB 병기의 경우 5년 생존율은 약 5%입니다.
- III기 췌장암의 5년 생존율은 약 3%입니다.
- 4기 췌장암은 5년 생존율이 약 1%입니다. 아직도, 암의 이 단계에 환자들에게 치료 옵션이 있기는 합니다.
이 생존율은 추정치일 뿐이며 어떤 개인에게 어떤 일이 일어날 지 예측할 수는 없습니다. 이러한 통계는 혼동을 줄 수 있으며 더 많은 질문을 하게 될 수도 있습니다. 특정 상황을 더 잘 이해하기 위해 의사와 상담하십시오.
Survival rates for neuroendocrine pancreatic tumors (treated with surgery)
For pancreatic neuroendocrine tumors (NETs), survival statistics by stage are only available for patients treated with surgery. These numbers come from the National Cancer Data Base and are based on patients diagnosed between 1985 and 2004.
- The 5-year survival rate for people with stage I pancreatic NETs is about 61%.
- For stage II pancreatic NETs, the 5-year survival rate is about 52%.
- The 5-year relative survival rate for stage III pancreatic NETs is about 41%.
- Stage IV pancreatic NETs have a 5-year survival rate of about 16%. Still, there are often treatment options available for people with these cancers.
In this database, the overall 5-year survival rate for people who did not have their tumors removed by surgery was 16%.
신경 내분비 췌장 종양의 생존율(수술로 치료한 경우)
췌장 신경 내분비 종양 (NET)의 경우, 단계별 생존율 통계는 수술을 받은 환자에게만 제공됩니다. 이 숫자는 National Cancer Data Base에 있으며 1985년에서 2004년 사이에 진단된 환자를 기준으로 합니다.
- 1기 췌장암 환자의 5년 생존율은 약 61%입니다.
- II기 췌장암의 경우 5년 생존율은 약 52%입니다.
- III기 췌장암의 5년 상대 생존율은 약 41%입니다.
- 4기 췌장암은 5년 생존율이 약 16%입니다. 아직도,이 암에 걸릴 수 있는 치료 옵션이 종종 있습니다.
이 데이터베이스에서 수술로 종양을 제거하지 않은 사람들의 전체 5 생존율은 16%입니다.
이번에는 비교적 최근 자료인 2013년도에 연구된 수술불가한 췌장암 환자의 TS-1과 gemcitabine의 비교 임상실험에 관해서 살펴보겠다. 이는 임상2상으로 진행된 췌장암 환자군을 대상으로 하였다. 그리고 한림대학교 의과대학에서 발표한 논문이다
Phase II trial of gemcitabine and S-1 for patients with advanced pancreatic cancer.
Song H1, Han B, Park CK, Kim JH, Jeon JY, Kim IG, Kim HJ, Jung JY, Kim JH, Kwon JH, Jang G, Kim HY, Kim HS, Choi DR, Zang DY.
Abstract
PURPOSE:
To evaluate the efficacy and safety of combined gemcitabine and S-1 as first-line chemotherapy for patients with locally advanced or metastatic pancreatic cancer.
목적 : 국소 진행 또는 전이성 췌장암 환자에서 1 차 항암 요법으로 gemcitabine과 S-1 병합 요법의 효능 및 안전성을 평가합니다 .
METHODS:
This study included patients who had been diagnosed with unresectable, locally advanced or metastatic adenocarcinoma arising from the pancreas, which was histologically or cytologically confirmed and involved at least 1 unidimensionally measurable lesion. The regimen consisted of intravenous 1,000 mg/m(2) gemcitabine on day 1 and 8 combined with oral S-1 on days 1-14 every 21 days. The dosage of S-1 was based on the body surface area (BSA) as follows: 40 mg bid (total 80 mg/day) for a BSA of <1.25, 50 mg bid (total 100 mg/day) for a BSA of ≥1.25 but <1.5, and 60 mg bid (total 120 mg/day) for a BSA of ≥1.5. Treatment consisted of at least 2 courses unless rapid disease progression was noted. The primary end points were the response and disease control rates, and the secondary end points were toxicity and survival.
방법 : 이 연구는 조직학적으로 또는 세포학적으로 확인된 췌장에서 발생한 절제 불가능하고 국소 진행성 또는 전이성 선암으로 진단 받고 최소한 1 개의 일차원 측정 가능한 병변을 포함하는 환자를 포함했다. 이 요법은 1일에 1,000 mg / m2의 젬시타빈을 1일과 8일에 정맥주사하고, 1 일-14일 동안에 구강 S-1을 함께 복용하여서 21을 한 주기로 구성하였고 S -1의 투여량은 다음과 같은 BSA (body surface area)를 기준으로 했습니다. BSA가 1.25, 50mg (총 100mg / 일)인 경우 40mg bid (총 80mg / day) BSA가 ≥1.5 일 때 ≥1.25, 그러나 <1.5, 그리고 60mg bid (총 120mg / day). 급속한 질병 진행이 확인되지 않는 한 치료는 최소한 2가지 코스로 구성되었습니다. 일차 평가 기준은 반응 및 질병 관리 비율이었고, 두번째 기준은 독성과 생존율이었다.
RESULTS:
Thirty-seven patients were enrolled between August 2005 and December 2010. The median number of chemotherapy cycles was 4 (range 1-28 cycles). Response to treatment could be evaluated in 31 patients. None of the patients showed complete response, but 5 achieved partial response. The response rate was thus 13.5 % [95 % confidence interval (CI) 2.7-24.3 %] in the intent-to-treat population. Sixteen patients (43.2 %; 95 % CI 27-59.5 %) showed stable disease, and the overall disease control rate was 56.8 % (95 % CI 40.6-72.9 %). For all 37 patients, the median progression-free survival was 4.6 months (95 % CI 1.8-7.6 month), and the median overall survival was 9.4 month (95 % CI 5.8-12.6 month). Chemotherapy-related grade 3/4 hematological toxicities were neutropenia (36.1 %), leucopenia (22.2 %), and anemia (13.9 %). The non-hematological toxicities were generally mild.
결과 :
2005년 8월과 2010년 12월 사이에 37명의 환자가 등록되었다. 화학 요법주기의 중앙값은 4주기 (1-28주기 범위)였다. 31명의 환자에 대한 치료 반응이 평가되었다. 완벽한 관해를 보인 환자는 한명도 없었고 5명이 부분적인 반응을 보였다 (partial response). 반응률은 치료 의도 집단에서 13.5% [CI 신뢰도 (CI) 2.7-24.3%]였다. 16명의 환자 (43.2%, 95% CI 27-59.5%)는 stable disease (종양이 더 자라지 않고 유지되는 것)을 보였고 전체 질병 통제 율은 56.8% (95% CI 40.6-72.9%)였다. 37명의 환자 모두에서 무진행 생존기간의 중앙값은 4.6개월 (95% CI 1.8-7.6개월)이었고 평균 생존기간 은 9.4개월(95% CI 5.8-12.6개월)이었다. 화학 요법과 관련된 3/4 등급의 혈액학적 독성은 호중구 감소증 (36. %), 백혈구 감소증 (22.2%), 및 빈혈 (13.9%). 비혈액학적 독성은 일반적으로 경미했다.
결론 :
젬시 타빈과 S-1 병합 요법은 진행성 췌장암 환자에서 효과적이고 편리하며 안전했다
CONCLUSIONS:Combination chemotherapy with gemcitabine and S-1 was effective, convenient, and safe in patients with advanced pancreatic cancer.
췌장암에 관한 치료의 가능성을 찾아보기 위하여서 논문을 뒤져보아도 대부분 옛날 논문들이고 전체적으로 회고적으로 연구한 논문은 거의가 2010년 전이다. 이는 그만큼 생존율이 낮아서 자료가 쌓이지 않기 때문에 생긴 문제이다. 최신에 2013년도 TS-1, gemcitabine 요법도 partial response 즉 조금이라도 줄었던 경우는 13.5%였고 종양이 더 크지 않고 일정기간 유지되었던 경우도 43%이다. 하지만 무진행 생존기간은 4.6개월인 것으로 보아서 4개월 이상 유지되지는 않았다는 이야기이다. 그리고 평균 생존기간은 9.4개월로 가장 일찍죽 은 사람이 5.8 개월이고 가장 오래 산 사람이 12.6개월이다.
앞서 이렇게 장황하게 여러 가지 논문을 실어 본 것은 이후의 한방치료와 비교하기 위해서이다. 췌장암 3강에서부터는 본원의 항암치료 결과를 임상적으로 비교해 보겠다.